- 欢迎来到细胞产业关键共性技术国家工程研究中心!
828号令+818号令:为生物医学新技术的双轨并行打通“任督二脉”
来源:细胞质量检测技术研发平台
建设单位:深圳科诺医学检验实验室
时间:2026-02-01
2026年1月27日注定会被载入史册。这天,一方面,中国科学院大学星际航行学院揭牌成立,标志着我国首个星际航行学院正式投入运行;另一方面,国务院正式发布了《中华人民共和国药品管理法实施条例》(国务院令第828号),并宣布自2026年5月15日起施行。
这一实施条例是《药品管理法》施行23年来的首次全面修订,对创新药物研发和监管做出了重大调整。从而,以细胞与基因治疗(CGT)技术为代表的生物医学新技术合规发展路径(即“双轨并行”模式)终于明晰:一条路径(“药”)归国家药品监督管理局(NMPA)监管,另一条路径(“术”)归国家卫健委监管,相当于为国内CGT产业的发展正本清源、打通“任督二脉”。
过去,一些试行性规定(如2015年《干细胞临床研究管理办法(试行)》和2023年《体细胞临床研究指引》)仅对非药品注册目的的研究进行了简单规范,且未明确商业转化及收费标准,导致合规路径并不完整。
相比之下,2017年底国家药监局(CDE)发布的《细胞治疗产品研究与评价技术指导原则》(试行)则为细胞治疗产品的药品注册指明了方向。随着818号令与828号令的陆续推出,我国生物医学新技术的“双轨制”监管体系正式成形。这意味着,今后CGT行业的发展将由“合规框架”与“创新引擎”双轮驱动,迎来更加规范与高效并重的新时代。
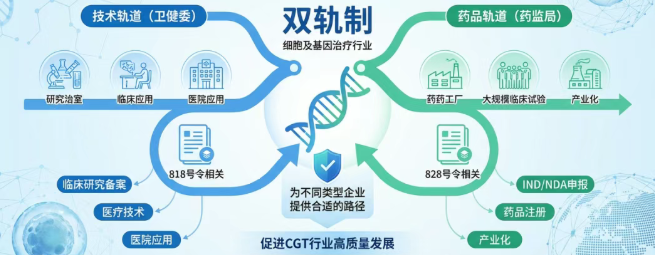
新修订的《药品管理法实施条例》(828号令)与《生物医学新技术临床研究和临床转化应用管理条例》(818号令),是我国生物医药领域的重要里程碑。前者从药品全生命周期的研制、生产到上市后监管等各环节进行细致规定,为细胞治疗等前沿产品提供了明确的法规支撑;后者则首次将干细胞治疗、基因治疗等技术纳入法定框架,开辟了医疗机构主导的技术转化路径。这两项法规共同构建了我国干细胞治疗“双轨制”监管体系——在监管逻辑上形成以人民健康为中心、鼓励创新与防控风险并重的格局。其中,“药品注册”路径由国家药监局负责,适用于可标准化批量生产的细胞制剂,强调质量体系与临床试验;“医疗技术转化”路径由卫健委负责,适配个性化、难以标准化的治疗操作,强调医院临床研究。正如业内分析所指出的,这一双轨模式明确了各自的监管主体和职责:药品类技术走“药”路线,医疗服务类技术走“术”路线。

《药品管理法实施条例》(828号令)自2026年5月15日起施行,是药监体系的一次“底层逻辑重构”。国家药监局表示,新条例完善创新支持体系,鼓励以临床价值为导向的药物研制与创新。对于CGT等创新生物药,条例中的多项条款给予实质激励和明确规范:
加速审批通道:条例明确设立突破性治疗药物、附条件批准、优先审评审批、特别审批等多种加速通道,大幅缩短临床试验周期和上市时间。这对于针对严重疾病、临床周期长的细胞治疗产品来说是一大利好,可以为患者提供“绿色通道”。
市场独占期激励:对符合条件的罕见病治疗用药物给予最长7年的市场独占期,对儿童用药给予最长2年独占期。这意味着,应用于罕见病或儿科领域的细胞治疗产品,可享受知识产权保护期,显著提高研发投入的回报预期。
临床数据与研发保护:条例规定,对于采用新化学结构的药品以及符合条件的其他药品,其未披露试验数据和其他数据提供保护,保护期最长6年。这为细胞治疗产品核心临床数据提供了法律屏障,激励企业投入更多资源进行创新研发。
生产灵活性:允许药品上市许可持有人(MAH)委托专业机构生产药品,并特别允许对生产工艺要求高的创新药进行分段生产。后者对CGT产业尤为重要:细胞产品工艺复杂,将细胞采集、修饰、扩增、制剂等环节分包给不同CDMO(合同定制生产)机构,既可提升效率又符合法规要求。
数据管理与溯源:条例规定生物制品生产全过程必须采集并留存完整数据。细胞治疗作为活体药物,对数据的完整性、可追溯性要求极高,该条款确保了生产过程质量可控。
全生命周期安全监管:条例强调上市许可持有人须建立药物警戒体系,持续监测不良反应,并定期进行上市后评价。鉴于细胞治疗可能存在长期风险,法规要求全程监管,确保患者安全。
综上所述,828号令虽然没有单独章节针对细胞治疗,但从创新研发到生产监管,全方位搭建起了细胞治疗产品的合规框架:既鼓励创新(快速通道、独占期激励、研发数据保护),又强化安全(GLP/GCP、数据留存、药物警戒)。
第818号令:构建生物技术临床转化路径
与828号令相辅相成的,是2025年9月28日发布、2026年5月1日起施行的《生物医学新技术临床研究和临床转化应用管理条例》(818号令)。这是我国首部专门规范生物医学新技术(包括细胞治疗、基因治疗、再生医学等)临床实施的行政法规。818号令的核心创新在于建立了“备案制+审批制”的双阶段管理体系,实现在鼓励创新与防控风险之间找到平衡:
临床研究阶段(备案制):在进行临床研究前,经非临床研究证明技术安全有效后,须通过医院伦理审查和学术审查,然后在5个工作日内向国家卫健委备案,便可开展研究。这一备案流程大幅缩短了新技术进入临床的时滞,激励科技成果迅速转化。同时,条例规定临床研究必须在经认证的三级甲等医疗机构进行,配备专业伦理委员会、学术委员会以及配套设施和人员;研究期间不得向受试者收费,强调安全第一、公益原则。
临床转化阶段(审批制):临床研究充分证明技术安全有效且符合伦理后,须经国家卫健委审批方可进入临床转化应用阶段。审批通过后,国家将公布该技术的正式名称、准入条件和操作规范,符合要求的医疗机构和人员才可开展收费服务。同时,条例对全生命周期的数据留存、样本追溯提出了严格要求,研究记录需保存30年,涉及子代的需永久保存,不得伪造或篡改数据。这一系列刚性条款筑牢了合规红线:违反规定可处以最高500万元罚款或没收违法所得10倍等重罚。
核心监管原则:条例明确提出“以人民健康为中心、防风险保安全、支持转化应用、强化责任落实”的四大原则。第一次在法规层面制度化地实现了“鼓励创新”与“防控风险”并重:通过简化备案流程提升创新活力,通过严格审批守住安全底线,既为具有实力的技术主体开辟“安全赛道”,又对违规行为形成强力威慑。
分类分级与双轨并行:条例明确定义了“生物医学新技术”的范畴,并厘清了与医疗器械和药品的监管边界,避免了重复监管或监管缺失。最重要的是,它正式确立了“双轨制”:即药品注册和医疗技术转化两条路径并行。对于可大规模生产、标准化程度高的技术,走NMPA的药品注册路线,需满足严苛的CMC标准和大规模临床试验,最终获得药品注册证书实现产品化商业化;而对于依赖临床操作流程、个性化强的技术,则走NHC的医疗技术路线,通过高质量的临床研究证明安全有效后,批准为医疗服务项目,以技术服务模式商业化。这种路径选择的战略意义重大:它要求企业根据技术特性和商业需求进行定位——追求快速落地的机构可优先走医疗技术路径,构建规模化细胞产品矩阵的企业则要强化药品路线。
总之,818号令为干细胞等前沿技术的临床研究与转化应用建立了明确流程,从临床前研究、安全性评价到研究伦理和受试者保护等各环节都提出了具体要求。这一条例标志着我国生物医药创新监管进入新阶段,为原本散乱的“野蛮生长”时代按下了刹车,让科学、规范、可持续的发展正式起航。
818号令与828号令的双剑合璧,为我国CGT产业插上了合规和创新的双翼。
医院端将深度绑定临床研究和技术转化:符合条件的三甲医院成为新技术研究的核心枢纽,需要强化伦理审查与全流程管理,不合规机构将被清理整顿。
企业端则面临战略抉择:要么走“药品路线”,加大研发投入、完善CMC体系、积累注册临床数据;要么走“医疗技术路线”,与三甲医院深度合作共建GMP级细胞制备平台,保证研究样本和数据质量。
CDMO/CRO等配套行业也将迎来巨大机遇和转型升级:传统生产服务需求将得到放大,同时合规咨询、伦理审查辅导等新需求爆发,行业需要从业者“量变到质变”地提升专业能力。
社会公众和患者未来可享受更安全透明的细胞治疗服务:已存储干细胞的用户可查询储存机构是否完成正规备案,接受治疗前可根据官方公布的技术名称、准入医院和操作规范判断项目合法性。
新政带来了前所未有的产业机遇:从研发投入到支付政策均出现“破冰”态势。国家卫健委已将“干细胞与器官修复”纳入重点研发计划,2025年投入4.3亿元;多地将细胞治疗纳入医保或普惠健康计划,报销比例可达65%;创新审批机制(如突破性治疗、紧急使用等)为危重患者打开绿色通道。这些都意味着,产业链上下游的CDMO、CRO、设备商和保险机构将迎来爆发式增长,临床研发和治疗效果转化的路径前所未有地清晰可见。
然而,严格监管也相应提高了运营成本:企业和医院要承受三甲资质、伦理审查、长期随访和30年数据留存等要求,投融资周期将进一步拉长;“概念+营销”的伪创新项目将被市场和监管出清,只有真正具有临床价值和安全性的技术才能生存下来。此外,真实世界数据的质量和完整性成为能否“术转药”的关键要素,任何试验数据的瑕疵都可能成为药监批准的拦路虎。
展望未来,2026–2027年将是我国CGT产业从“政策红利期”迈向“价值兑现期”的关键窗口。随着双轨政策的落地,更多成熟的干细胞疗法有望进入国家医保目录,极大提升可及性;通用型干细胞药物将在规模化生产中继续降本增效,为患者提供更可负担的治疗方案。同时,基于长期随访和真实世界研究(RWS)的疗效评估体系将日趋完善,成为评价细胞治疗安全性和有效性的核心依据;行业集中度有望提升,只有具备“技术+临床+合规”三位一体能力的领军机构才能在激烈竞争中脱颖而出。
最后要强调的是:政策并非束缚,而是为真正有价值的疗法铺设轨道。对已存储干细胞的患者而言,这意味着更高的安全保障和更透明的服务标准;对产业同仁而言,则意味着在创新与合规之间找到最佳平衡。正如有业内专家所言:“当野蛮生长的时代结束,科学、规范、可持续的发展才真正开始”。在国家双轨监管体系的护航下,中国CGT产业正迎来高质量发展的黄金时代,每一步合规的前行都将为人类健康事业增添更多希望。
