- 欢迎来到细胞产业关键共性技术国家工程研究中心!
CELLALL细胞全生命周期追溯解决方案落地,完美契合细胞治疗产品GMP规范
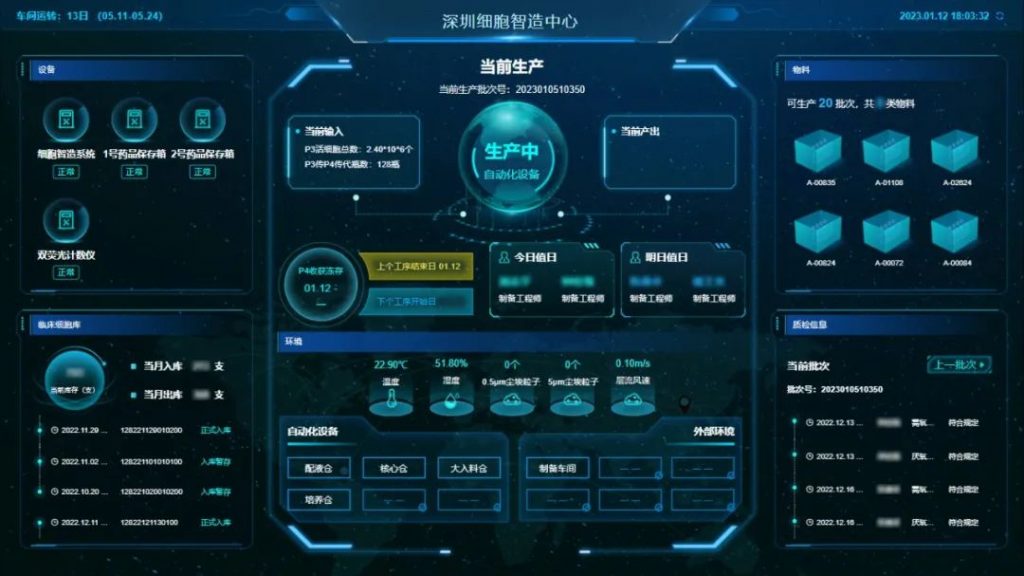
来源:细胞全生命周期管理平台
承载单位:个体化细胞治疗技术国家地方联合工程实验室(深圳)
时间:2023-01-30
2022年底,国家药监局正式发布了《细胞治疗产品生产质量管理指南(试行)》。该指南明确:我国细胞治疗产品领域当前处于快速发展的阶段,为进一步推进该领域的健康发展,基于当前的科学认知以及针对细胞治疗产品相关技术的发展现状,提出本指南,主要为细化和完善细胞治疗产品产业化阶段生产质量管理方面的技术要求,旨在为细胞治疗产品生产企业提供指导意见,同时,也可作为监管机构开展各类现场检查的重要参考。
指南对细胞产品溯源做了明确的要求,具体如下:
第十一章【产品追溯系统】第(一)条 企业应当建立产品标识和追溯系统,确保在供者材料运输、接收以及产品生产和使用全过程中,来源于不同供者的产品不会发生混淆、差错,确保供者材料或细胞与患者之间的匹配性,且可以追溯。
该系统宜采用经验证的计算机化系统,应当可以实现对产品从供者到患者或从患者到供者的双向追溯,包括从供者材料接收、运输、生产、检验和放行,直至成品运输和使用的全过程。
第十一章【产品追溯系统】第(二)条 企业应当对每一个供者编制具有唯一性的编号(或代码),用于标识供者材料和产品。
细胞药品追溯相关政策及法规
01、2016年9月,国家食品药品监管总局下发《总局关于推动食品药品生产经营者完善追溯体系的意见》(食药监科〔2016〕122号),继续推进药品追溯系统的建立和完善,鼓励药品生产经营者运用信息技术建立药品追溯体系;鼓励行业协会组织企业搭建药品追溯信息查询平台,为药品监管部门提供数据支持,为药品生产经营者提供数据共享,为公众提供信息查询。
02、2017年2月,商务部等七部门联合印发《关于推进重要产品信息化追溯体系建设的指导意见》,其中对药品追溯体系建设提出了四大要求:
第一,巩固提升中药材流通追溯体系,升级改造中药材流通追溯管理中央平台,促进不同药品追溯系统信息互通共享;
第二,推动药品生产流通企业落实主体责任,使用信息化技术采集留存原料来源、生产过程、购销记录等信息,保证药品的可追溯;
第三,扩大药品追溯监管覆盖范围,逐步实现全部药品从生产、流通到使用全程快速追溯;
第四,建立健全药品追溯管理机制。
这一指导性的具体意见为建立健全和推进药品追溯体系制度建设进一步指明了方向,具有更强的可操作性。
03、2018年8月24日,国家药监局发布《关于药品信息化追溯体系建设的指导意见(征求意见稿)》,明确药品上市许可持有人MAH(包括持有药品批准文号的药品生产企业)是药品追溯体系建设的责任主体;允许多种编码并存,企业可自主选择;监管部门负责监督指导,同时推进追溯信息的互联互通,到2022年底,基本完成药品信息化追溯体系全覆盖。
04、2018年10月31日,国家药监局正式下发《关于药品信息化追溯体系建设的指导意见》(国药监药管〔2018〕35 号),标志药品追溯体系再次重出江湖,明确要求药品上市许可持有人、生产企业、经营企业、使用单位通过信息化手段建立药品追溯系统,及时准确记录、保存药品追溯数据,形成互联互通药品追溯数据链,实现药品生产、流通和使用全过程来源可查、去向可追,有效防范非法药品进入合法渠道,确保发生质量安全风险的药品可召回、责任可追究等。
05、2019年4月19日,国家药监局下发《药品信息化追溯体系建设导则》和《药品追溯码编码要求》两项信息化标准,对药品追溯码的编码原则,编码对象、基本要求、构成要求、载体基本要求、发码机构基本要求和药品上市许可持有人、生产企业基本要求等提出了具体的要求。
06、2019年8月23日,国家药监局印发了《疫苗追溯基本数据集》,《疫苗追溯数据交换基本技术要求》和《药品追溯系统基本技术要求》3项标准,重点规范了药品追溯系统技术要求,并为疫苗药品追溯体系建设提供科技支撑依据。
07、2019年12月1日,新《药品管理法》正式生效,正式将药品追溯作为我国药品管理的基本制度,药品追溯制度是实现药品风险管理、全程管控、社会共治的重要手段。
08、2020年3月6日,国家药监局印发了《药品上市许可持有人和生产企业追溯基本数据集》、《药品追溯数据交换基本技术要求》、《药品经营企业追溯基本数据集》、《药品使用单位追溯基本数据集》、《药品追溯消费者查询基本数据集》5项信息化标准。
09、2021年4月27日,国务院办公厅发布了关于全面加强药品监管能力建设的实施意见,其中第(十三)条 完善信息化追溯体系:制定统一的药品信息化追溯标准,实行药品编码管理,落实药品上市许可持有人追溯责任。构建全国药品追溯协同平台,整合药品生产、流通、使用等环节追溯信息,从疫苗、血液制品、特殊药品等开始,逐步实现药品来源可查、去向可追。逐步实施医疗器械唯一标识,加强与医疗管理、医保管理等衔接。发挥追溯数据在风险防控、产品召回、应急处置等工作中的作用,提升监管精细化水平。
10、2022年1月6日,国家药监局发布了《药品生产质量管理规范-细胞治疗产品附录(征求意见稿)》,其中第四十七条【产品追溯系统】:企业应当建立产品标识和追溯系统,确保在供者材料运输、接收以及产品生产和使用全过程中,来源于不同供者的产品不会发生混淆、差错,确保供者材料或细胞与患者之间的匹配性,且可以追溯。
该系统宜采用经验证的计算机化系统,应当可以实现对产品从供者到患者或从患者到供者的双向追溯,包括从供者材料接收、运输、生产、检验和放行,直至成品运输和使用的全过程。
11、2022年10月31日,国家发展改革委发布了《“十四五”生物经济发展规划》,这是我国首部生物经济的五年规划,凝聚了生物经济发展的具体任务。其中第四章中提出了实现药品、疫苗从生产到使用全生命周期管理,构建药品追溯体系。并利用信息技术支撑新药研制,对新药研制过程进行全程监管,提升制药装备的自动化、数字化和智能化水平。
12、2022年5月10日,国家药监局核查中心正式发布了《细胞治疗产品生产质量管理指南(试行)》,其中第十一章明确提出了细胞产品追溯系统的建设要求。
随着药品追溯相关政策及法律法规的密集出台,细胞药品全生命周期追溯已成必然。作为细胞产业关键共性技术国家工程研究中心八大平台之一的细胞全生命周期管理平台,历经多年自主研发,已打造出成熟可落地的细胞全生命周期追溯解决方案,完美契合最新的细胞治疗产品生产质量管理规范以及NMPA药品追溯体系架构,实现对细胞产品从供者到患者或从患者到供者的双向追溯,助力细胞药品生产、流通和使用全程监管,为药品上市许可证持有人提供有力的产品监管工具,为行业、政府监管部门、公众提供权威的细胞药品公共数据平台服务。
关于细胞全生命周期管理平台
2022年6月,国家发改委正式发文批复同意由深圳科诺医学检验实验室牵头组建“细胞产业关键共性技术国家工程研究中心”,通过国际资源整合和协同攻关,重点建设8大功能平台,促进细胞产业基础高级化和产业链现代化。
作为该工程研究中心八大平台之一的细胞全生命周期管理平台,是一个创新平台,负责搭建CGT产业全生命周期溯源平台,以赋能行业、便利监管。
主要研发内容
围绕细胞创新链与产业链的研发、生产、流通、应用涉及的全生命周期环节,通过自动化、智能化、数字化技术,打造细胞全生命周期追溯系统,为科研、生产、监管等不同节点提供公共数据平台服务。通过为细胞分配一物一码身份证,促进产业链上不同业务环节的数据融合,保障细胞创新链与产业链全流程可视化、数字化、可追溯,助力工业信用体系的形成,为研发生产赋能,为监管减负。
主要任务
通过一体化平台架构设计,集中进行数据管理和数据共享,助力业务流程优化,降低运营成本,提升协同效率,促进数据共享,建设可信体系,实现包容审慎的监管,保障细胞安全。最终促进细胞产业基础高级化,产业链现代化,为细胞新产业、新服务、新业态保驾护航。
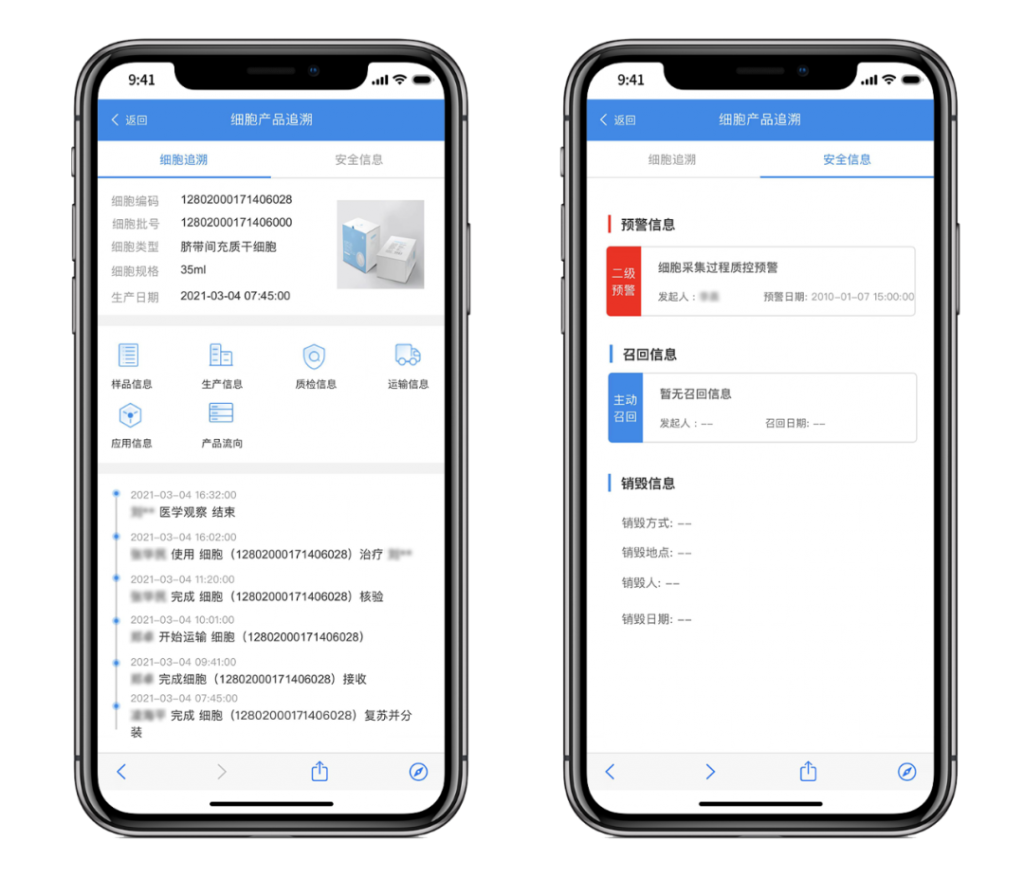
细胞全生命周期管理平台历经多年自主研发,依据《细胞治疗产品生产质量管理指南(试行)》及NMPA《药品追溯系统基本技术要求》、《药品追溯码编码要求》进行设计,凝聚了多项发明专利及软件著作权,发布细胞全生命周期追溯解决方案,支持从供体材料接收、运输、生产、检验和放行,直至成品运输和使用的全过程中对产品从供者到患者或从患者到供者的双向追溯,为细胞治疗产品合规上市提供有力的工具,最终确保细胞来源可查,去向可追,风险可控,责任可究,保证细胞药品质量的“真实、可靠、可追溯”。助力细胞药品生产、流通和使用全程监管,最终帮助细胞药厂实现生产效能最大化,追溯成本最小化,同时为药品监管部门,为公众提供权威的细胞药品公共数据查询服务。
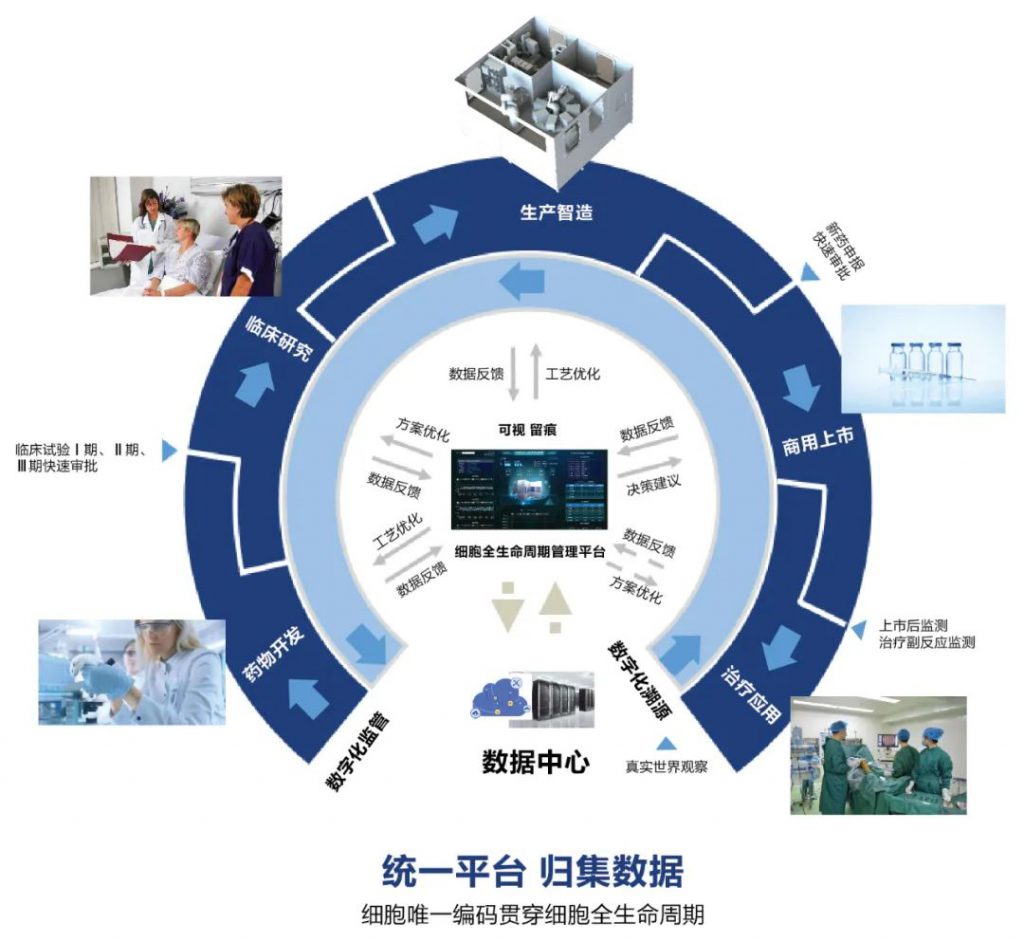
CELLALL追溯解决方案相关系统介绍
CELLALL细胞全生命周期追溯解决方案可用于细胞公司、科研院所,根据客户内部信息化建设程度,可分为三种实施方式:
【集成模式】
与企业现有信息系统集成及数据对接,全自动化的方式生成追溯数据。
【独立实施】
勿需集成其它系统,由人工录入及复核数据。
【一站式实施】
直接采用细胞全生命周期追溯解决方案中的一系列自动化软件进行实施,包括且不限于如下软件,并根据客户公司的业务规模及管理要求的复杂度,组合本方式中不同的自动化软件,分为专业版和标准版:
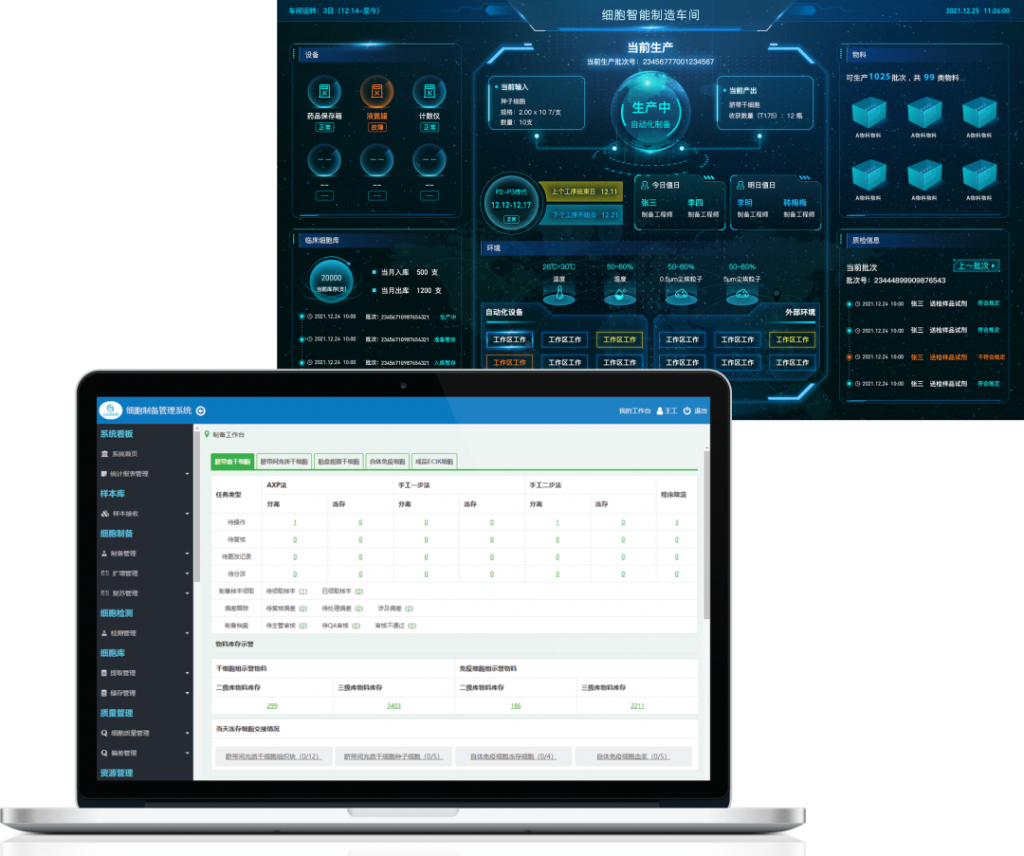
GMP生产自动化软件
基于GMP合规要求和全面的细胞质量控制策略,协助细胞生产企业完成从传统制备管理迁移到数字化的细胞制备生产管理。涵盖细胞生产全过程质量因素管理,可视化、合规、全程可溯,适应远程交互审计。
生物样本库自动化软件
协助解决管理者遇到的样本取放操作出错、细胞等样品位置不可视、台账查询不便捷及样本质量难以大规模监控等管理问题。系统以图形化方式进行管理,可以自动化储存及管理样本,实时展示样本物理位置,并可进行库存智能预警。
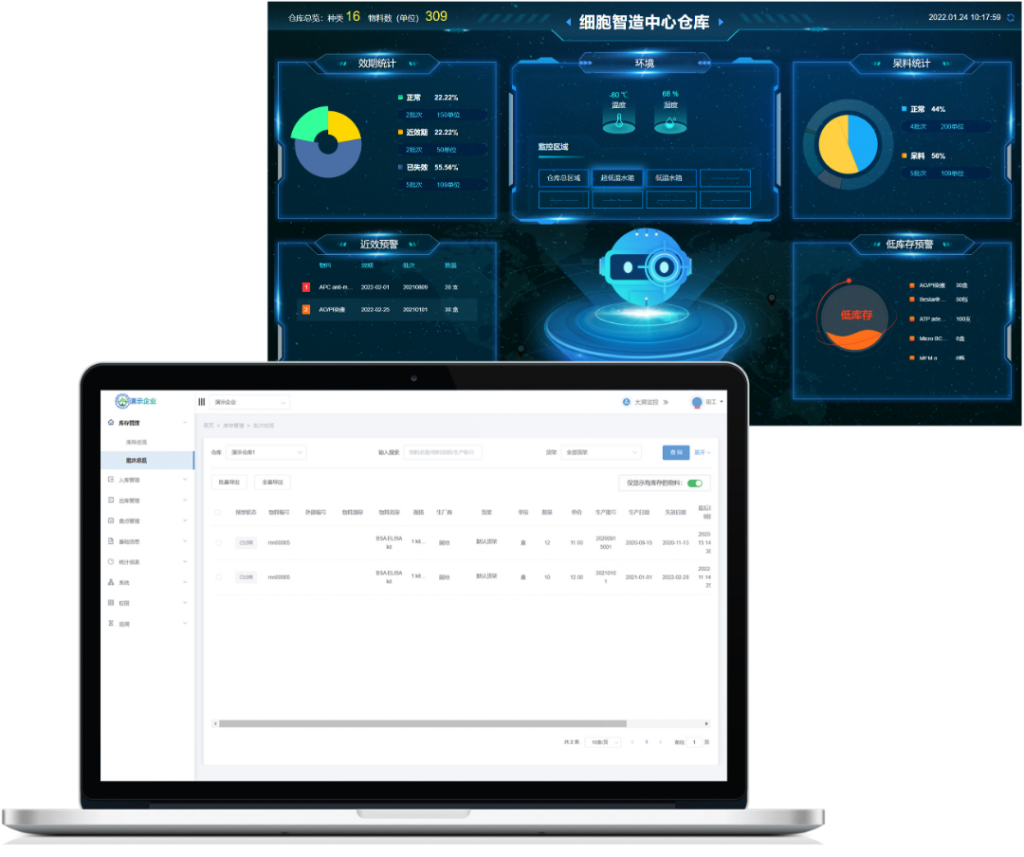
自动化仓储软件
集成物联网传感器的机器人自动出入库技术和传感终端,协助医药研发及生产类企业解决库存规划难、管理投入大、不易溯源及应对监管难等问题,实现物料仓储的数字化、智能化升级。
设备自动化管理软件
用于制药过程的数字化设备管理,实现了GMP对设备管理的要求,用户能够快捷、准确、全面的掌握设备状况、完成设备日常运维、检修、计划等管理工作。
专业人员管理软件
管理生物医药行业人员上岗要求及支持岗位技能考核、每年的继续教育,确保认证资质等与岗位匹配,并可溯源。
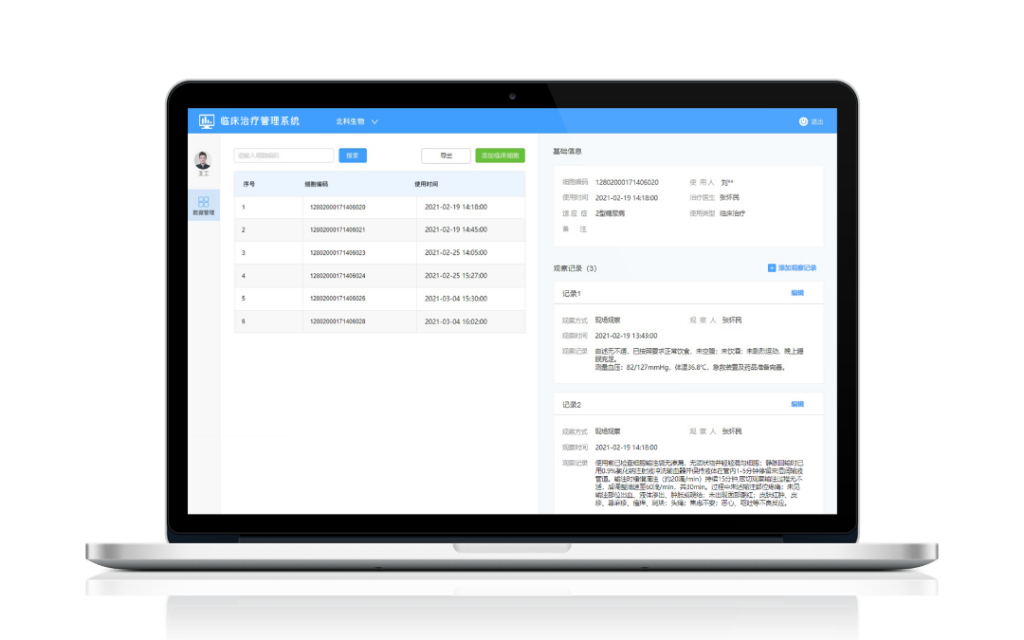
临床数据自动化采集软件
通过数字化方式自动采集患者临床数据、实时报告症状并进行监测,相关数据也可反馈至生产端,用于方案优化,工艺调整。
物流溯源追踪软件
对细胞产品运输各过程环节进行实时/历史数据监测、同步记录和实时环境预警,保障冷链运输过程安全进行。
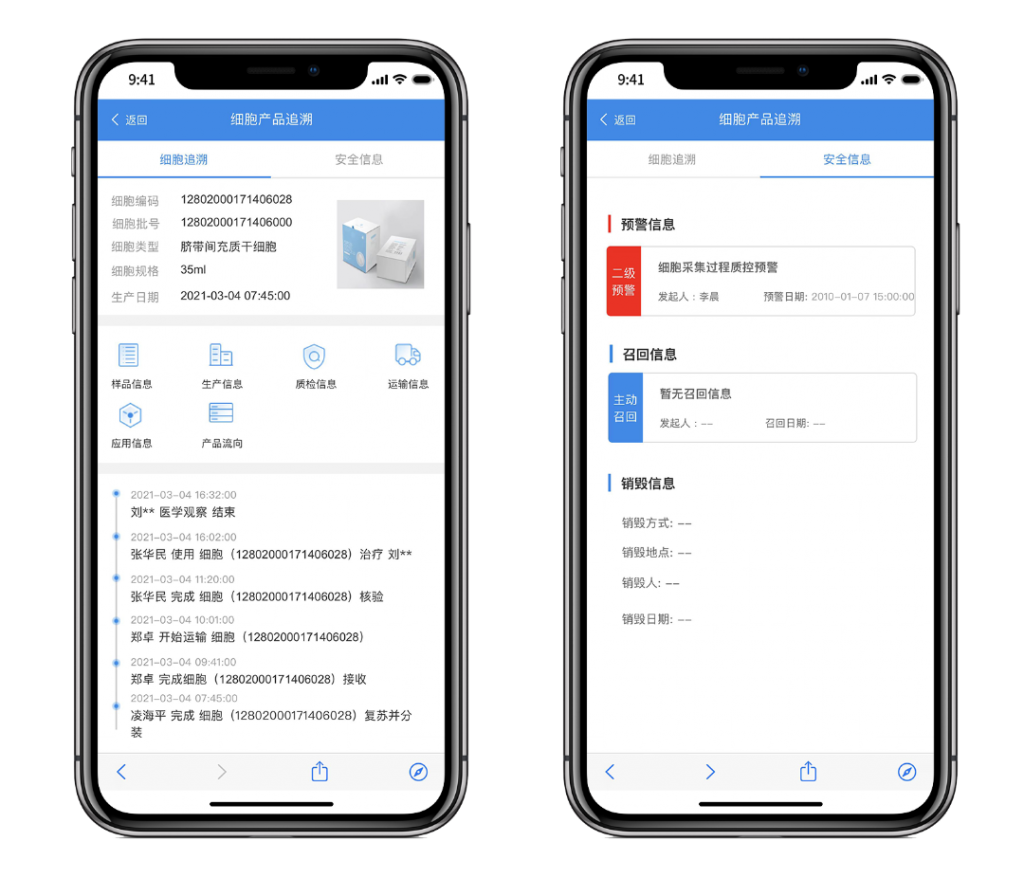
CELLALL细胞全生命周期溯源软件
依据《细胞治疗产品生产质量管理指南(试行)》进行建设,支持从供体材料接收、运输、生产、检验和放行,直至成品运输和使用的全过程中对产品进行双向追溯,为您的细胞治疗产品合规上市提供有力的工具。
2022年,本解决方案在深圳某龙头细胞公司实施落地,完美实现该公司细胞药品从生产端至临床端人机料法环全生命周期追溯。